邻近标记技术(PL):探索生物分子相互作用的前沿工具
在生命科学领域,深入理解生物分子间的相互作用对于揭示细胞功能和生命活动的机制至关重要。传统的检测方法如共免疫沉淀(Co-IP)存在诸多局限性,例如难以检测瞬时和弱相互作用,以及对有效抗体的依赖。邻近标记(Proximity Labeling, PL)技术的出现为克服这些挑战提供了新的解决方案。PL技术通过将目标蛋白与工具酶标签融合,在外部刺激(如生物素、过氧化氢等)下将邻近小分子探针转化为活性中体,与邻近蛋白交联,进而富集和分析相互作用蛋白。自2012年首次应用于哺乳动物细胞以来,PL技术不断拓展应用领域,包括RNA-蛋白相互作用、小分子-蛋白相互作用、细胞表面蛋白相互作用及亚细胞蛋白运输等。本文综述了PL技术在这些新兴领域的最新进展,探讨其在不同生物学问题中的创新应用,推动生命科学领域的发展。
一、PL技术原理
蛋白邻近标记的基本原理是将工具酶标签与目标蛋白融合,利用工具酶的活性将生物素标记到目标蛋白临近的其他互作蛋白上。随后,通过亲和素-生物素的高度特异性结合将带有生物素标记的互作蛋白进行纯化富集,并进行质谱检测分析以鉴定目标蛋白的互作蛋白。
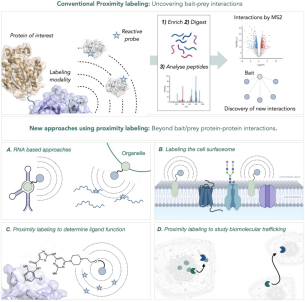
PL技术的传统以及创新应用
二、PL用于RNA研究
在遗传信息传递的舞台上,RNA起着至关重要的作用,然而其与蛋白之间的相互作用却一直是研究的难点。PL技术的出现为这一领域带来了转机,先前的研究表明,APEX技术通过将APEX2酶靶向特定细胞区域,在H2O2和生物素标记的苯酚作用下,产生活性中间体,成功标记邻近的蛋白和RNA,帮助绘制出RNA在细胞内的分布图谱及其与蛋白的相互作用网络。此外,单线态氧光敏化标记技术如CAP-seq和HALO-seq,利用光敏蛋白或染料产生单线态氧,氧化鸟嘌呤并引入烷基,实现了RNA的原位标记,为研究RNA的精细定位和功能提供了新的视角。而RNA导向的PL技术更是突破性地通过引导PL至目标RNA,深入探究特定RNA如何调控细胞过程,为 RNA生物学研究开辟了新的途径。
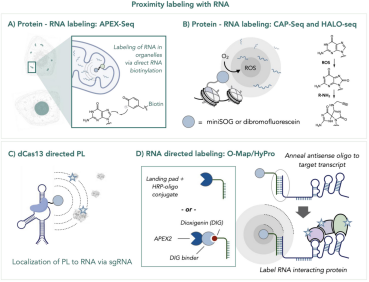
基于RNA的PL技术
三、PL用于小分子-生物分子相互作用
在药物研发的研究中,确定小分子药物与生物分子靶标的相互作用是关键一步。PL技术在这方面展现出巨大的潜力。配体导向的PL方法,如μMap技术,通过将小分子配体与铱催化剂连接,经光激发后激活探针,实现对小分子配体周围生物分子的无序列特异性标记,为药物靶点鉴定提供了高效手段。同时,配体干扰的PL方法则通过比较有无小分子配体存在下POI的相互作用组变化,揭示配体如何影响蛋白-蛋白相互作用,为理解药物机制和优化药物设计提供了宝贵的线索,助力科学家们在药物研发中精准定位靶点。
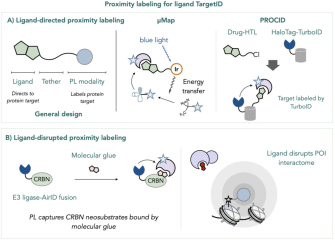
基于小分子的PL技术
四、PL用于细胞表面蛋白研究
细胞表面蛋白负责细胞间的信号传递和通信。PL技术为研究细胞表面蛋白及其相互作用提供了创新方法。一方面,通过将PL酶与膜蛋白融合,可特异性地标记细胞表面蛋白,绘制出细胞表面组的详尽图谱。另一方面,基于细胞表面糖链的标记方法,如将APEX2与糖链结合蛋白融合,或通过代谢引入含叠氮基的唾液酸标记细胞表面蛋白,为探究细胞间通信和细胞表面动态变化提供了有力工具,揭示细胞如何感知外界环境并做出响应。
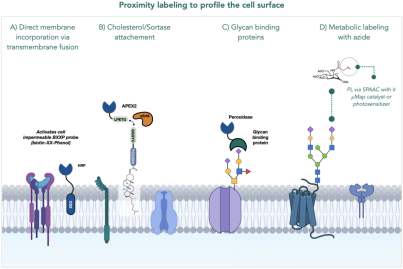
基于细胞表面蛋白的PL技术
五、PL用于蛋白质运输
蛋白质在细胞内的运输过程对于细胞功能的正常发挥至关重要。PL技术巧妙地应用于蛋白运输研究,如TransitID方法结合TurboID和APEX2等PL技术,通过在不同时间点对蛋白进行标记,追踪蛋白在细胞内或细胞间的运输轨迹。这使得研究人员能够实时观察蛋白在细胞应激等条件下如何从一个细胞区室移动到另一个,为理解蛋白运输机制和细胞内物流网络提供了全新的视角。
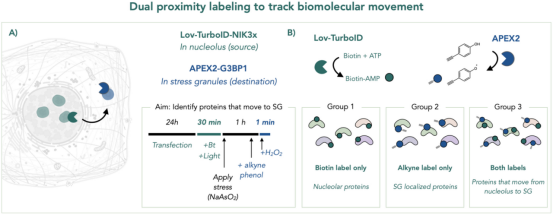
基于蛋白质运输的PL技术
六、总结
在生命科学领域,深入理解生物分子间的相互作用对于揭示细胞功能和生命活动的奥秘至关重要。传统的检测方法(如共免疫沉淀及其衍生技术)存在诸多局限性,例如难以检测瞬时和弱相互作用,以及对有效抗体的依赖,这些限制了对生物分子相互作用的全面研究。邻近标记(Proximity Labeling, PL)技术的出现为克服这些挑战提供了新的解决方案。PL技术通过将目标蛋白与催化剂融合,在外部刺激下将邻近小分子探针转化为活性中间体,与邻近蛋白交联,进而富集和分析相互作用蛋白。自2012年首次应用于哺乳动物细胞以来,PL技术不断发展,其应用领域也不断拓展,包括研究RNA-蛋白相互作用、小分子-蛋白相互作用、细胞表面蛋白相互作用及亚细胞蛋白运输等。这些进展表明,PL技术正在成为生物分子相互作用研究中不可或缺的工具,并将继续推动生命科学领域的发展。未来,随着PL技术的进一步创新和优化,预计其在更广泛的生物学场景中将发挥更大的作用,为生命科学的深入研究提供新的可能性。
